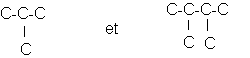
TP CO3 : De la représentation de Lewis à l'écriture topologique :
I/Représentation de Lewis : rappel
a)Ecrire la représentation de Lewis de la molecule de formule brute C2H6 . Même question avec C3H8 .
b)Ecrire la représentation de Lewis d'une molécule qui possède une chaîne de 6 atomes de carbone . En déduire sa formule brute .
c)Dire pourquoi , dans les exemples précédents, la formule développée est identique à la représentation de Lewis .
II/Squelette carbonné :
Le squelette carboné d'une molécule est l'enchaînement des atomes de carbone de la molécule .
a)Un squelette carbonné est-il une représentation de Lewis d'une molécule ?
b)Quel est le squelette carbonné de la molécule de butane C4H10 et celui de la molécule de méthane ?
c)Quelle est la formule développée de l'hydrocarbure dont le squelette carboné est C-C-C-C-C ?
d)Même question avec :
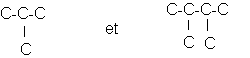
e)Proposer plusieurs squelette carbonés pour les molécules possédant 5 atomes de carbone .
III/Ecriture topologique :
On passe d'un squelette carboné à une écriture topologique en ne traçant que les liaisons chimiques entre les atomes de carbone du squelette carboné . L'exemple suivant illustre l'équivalence entre les deux ecritures :
![]()
a)Donnez une écriture topologique de la formule suivante :
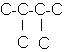
b)Même question pour C3H8
c)Pourquoi n'utilise t-on jamais d'écriture topologique pour le méthane ?
d)Donnez les formules développées et semi-développées de la
molécule dont l'écrirure topologique est : ![]()
e)Construire la molécule en utilisant une boîte de modèles moléculaires . Nommez la molécule .
IV/Equivalences d'écritures topologiques :
Deux écritures topologiques sont équivalentes si l'on peut passer de l'une à l'autre en modifiant l'orientation des petits segments .
a)Montrer que les écritures suivantes sont équivalentes :
![]()
b)Les écritures topologiques suivantes sont-elles équivalentes ?
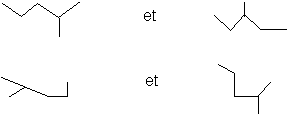
c)Proposez trois écritures topologiques non équivalentes correspondant à la formule brute C5H12 .
V/Isomères :
Deux molécules sont dites isomères si elles ont la même formule brute , mais des formules développées différentes .
a)Montrer que l'on peut êcrire deux molécules isomères de formule brute C4H10 .
b)Les alcanes ont pour formule brute générale CnH2n+2 . Combien d'alcanes isomères non cycliques possèdent 5 atomes de carbone ?
c)Montrer que les hydrocarbures suivants sont des isomères :
![]()
correction :
I/a-Représentations de Lewiw des formules brutes C2H6 et C3H8
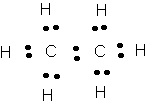
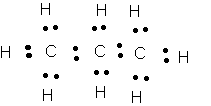
b)- 6 atomes de carbone : formule brute C6H14
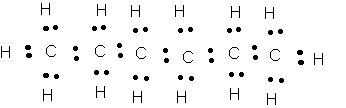
c)La formule développée est identique à la représentation de Lewis dans les exemples précédents car il n'y a pas de doublets non liants .
II/a- Un squelette carboné n'est pas une représentation de Lewis de la molécule car on ne représente que les atomes de carbone .
b-
Squelettes carbonés du méthane et du butane :
C et ![]()
c)
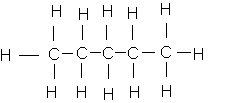
d)
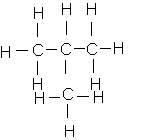
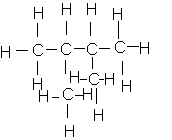
e)Squelettes avec 5 atomes de carbone :
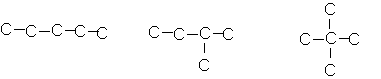
III/-a :
![]()
b:
![]()
c: Dans le méthane il n'y a pas de liaison C--C
d:
* formule semi-développée :
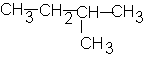
* formule développée :
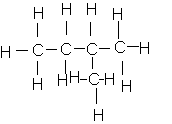
e:2-méthylbutane
IV/a:On peut passer d'une forme à l'autre en faisant pivoter ou en étirant les liaisons sans les "casser" : les 4 représentations correspondent par conséquent à la même molécule .
b:les deux premières sont équivalentes et les deux autres aussi
c:
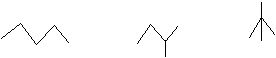
IV/a: formules topologiques des deux isomères .

b: 3 isomères (voir II-e)
c: la première molécule est le cyclohexane de formule brute C6H12
la seconde est l'hex-1-ène , de même formule brute que le cyclohexane .